个体会经历衰老和死亡,而生命谱系长存,这归因于生殖细胞和体细胞之间的分工(germline-soma separation)。生殖细胞负责生命延续,而起支持作用的躯体则承担损伤,是种系延伸的“耗材”(disposable soma)。相应地,大多数体细胞随着“年龄”增长,端粒损耗、DNA损伤和表观遗传漂变等“衰老印记”不断累积,细胞功能下滑。然而,胚胎干细胞的存在似乎挑战了这一范式,它可以永久增殖并保持分化能力,它如何绕过这些限制?是细胞个体的永生奇迹还是谱系的生存策略?尽管胚胎干细胞的端粒维持机制已被充分阐明,但其如何避免累积的分子损伤仍不清楚。
答案或许藏在一个意想不到的细胞行为中——2026年2月3日,广医-广州生物院联合生科院/广州国家实验室闵明玮团队和张满团队的合作研究首次揭示,小鼠的胚胎干细胞(mESC)通过不对称分裂来帮助细胞谱系永葆年轻。这项新研究“Asymmetric Division in a Two-Cell-Like State Rejuvenates Embryonic Stem Cells”发表在Cell Research上:利用长时程活细胞成像技术,追踪单个mESC谱系的命运和DNA损伤状态,发现mESC积累DNA损伤后,会自发性进入二细胞样状态(2C-like state),在该状态下,多数细胞产生不对称的DNA损伤分离,富集了较多DNA损伤的子代细胞谱系最终走向死亡,而其姐妹谱系则重获多能性、减少DNA损伤并比长期没经历过2C-like state的mESC更高效贡献嵌合体。进一步的功能干扰表明,阻止进入2C-like state会严重损害mESC的自我更新。这一新发现强调了不对称分裂是维持谱系延续的关键,不仅为研究哺乳动物细胞的细胞衰老和更新提供了一个潜在的模型,也为癌细胞的永生化机制提供新思路。

干细胞耗竭一直以来是再生医学的重大挑战,而胚胎干细胞的存在则打破衰老界限,解析其“永生之谜”或许会为此带来新突破。mESC在正常培养条件下,会自发进入2C-like state1,其标志是MERVL和Zscan4等基因的表达。有趣的是,当敲低Zscan4的表达2或清除MERVL阳性细胞3时会引发mESC的培养危机,而诱导Zcan4高表达,则增强mESC的多能性4,这表明2C-like state宛如“青春之泉”。然而,矛盾的是,处于2C-like state的mESC往往表现出更高的复制压力、DNA损伤和细胞凋亡,这凸显了我们对2C-like state如何促进mESC谱系更新的理解存在不足。
研究人员通过MERVL::GFP报告系统来实时追踪单个mESC进出2C-like state前后的命运变化,发现多数mESC进入2C-like state后会产生两支不同命运的子代谱系,一支经历MERVL::GFP越来越亮,并最终死亡;另一支经历MERVL::GFP越来越弱,经历多代分裂后最终回到mESC(Video)。同时,利用DNA损伤的报告系统,观察到DNA损伤在该过程中也发生了不对称分配,遗传较多损伤的子代通常走向MERVL::GFP荧光越来越亮的死亡命运,而遗传较少损伤的子代则退出2C-like state,回到mESC。为了进一步探究这群经历不对称分裂后退出2C-like state的mESC是否在功能上变得“更年轻”。研究人员使用了优雅的荧光蛋白计时器系统,得以分选出刚刚退出2C-like state的mESC,并与长期未进入2C-like state的mESC相比,结果显示前者具有较少DNA损伤,较高多能性基因表达,以及更好的体外克隆形成与体内嵌合能力(图)。胚胎干细胞通过智慧的牺牲与分配,让谱系在个体的减法中做加法的延续,这或许是细胞谱系对抗熵增的终极武器。
Video: mESC进入2C-like state后(MERVL::GFP+)产生不对称的子代细胞命运5
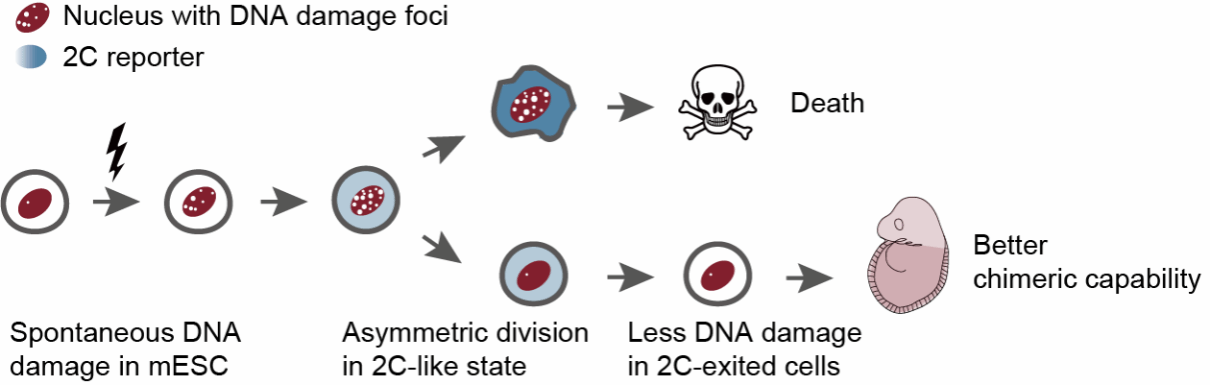
图:在2C-like状态下重塑mESC谱系的不对称分裂模型5
广医-广州生物院联合生科院/广州国家实验室闵明玮、张满研究员为该文章的共同通讯作者。博士生王鑫怡(广州医科大学)、付洪和孙庆杨(上海科技大学)、助理研究员黄博言和科研助理徐哲(广州国家实验室)为该文章的共同第一作者。广医-广州生物院联合生科院为本文第一单位。该工作得到国家自然科学基金、广东省重大人才工程引进创新创业团队项目、广州国家实验室专项项目、广东省基础与应用基础研究基金联合基金(省市联合)专项项目等的资助。
正文下载:https://rdcu.be/e12cy
全文链接:https://www.nature.com/articles/s41422-026-01221-z
闵明玮实验室网站:https://minlab.ac.cn/
参考文献:
1. Macfarlan, T. S. et al. Embryonic stem cell potency fluctuates with endogenous retrovirus activity. Nature 487, 57–63 (2012).
2. Zalzman, M. et al. Zscan4 regulates telomere elongation and genomic stability in ES cells. Nature 464, 858–863 (2010).
3. Du, Z. et al. The totipotent 2C‐like state safeguards genomic stability of mouse embryonic stem cells. Journal Cellular Physiology jcp.31337 (2024) doi:10.1002/jcp.31337.
4. Amano, T. et al. Zscan4 restores the developmental potency of embryonic stem cells. Nat Commun 4, 1966 (2013).
5. Wang, X. et al. Asymmetric division in a two-cell-like state rejuvenates embryonic stem cells. Cell Res 1–14 (2026) doi:10.1038/s41422-026-01221-z.
