近日,广医-广州生物院联合生科院袁慎立团队联合山东大学生殖医学与子代健康全国重点实验室吴克良团队、黄涛团队以及广妇儿优生围产研究所刘超团队在国际期刊Advanced Science发表题为 “The Landscape and Regulation of Histone Crotonylation in Mammalian Gametes and Early Embryos”的研究论文。

该研究系统绘制了哺乳动物配子和早期胚胎中代表性组蛋白巴豆酰化修饰H3K18cr的高分辨率图谱,揭示了其在受精后发生的大规模重编程过程,并阐明了组蛋白巴豆酰化与合子基因组激活(ZGA)及早期胚胎发育之间的密切联系。研究表明,H3K18cr 在小鼠精子中显著富集,但在MII卵母细胞中则几乎缺失,并在受精后迅速重建。
进一步分析发现,H3K18cr 在合子到两细胞阶段经历了由宽峰向经典窄峰的全局转变,这一过程依赖于minor ZGA。当研究人员利用 α-鹅膏蕈碱抑制胚胎转录后,这种由宽峰向窄峰的转变明显受阻,提示早期转录激活是驱动 H3K18cr 重塑的关键因素。与此同时,H3K18cr 还呈现出显著的亲本来源差异:合子阶段母源信号更强,之后随着胚胎发育推进逐渐趋于平衡。
机制研究进一步发现,HDAC1复合体介导的组蛋白去乙酰化活性对H3K18cr的正常重编程至关重要。抑制HDAC1活性不仅增强组蛋白乙酰化水平,也会阻碍H3K18cr从宽峰向窄峰的转换,说明组蛋白巴豆酰化与乙酰化之间存在重要的功能性交叉调控。
研究还表明,若通过巴豆酸处理扰乱这一转变过程,将导致主要ZGA基因表达受损,并影响囊胚发育进程。此外,研究团队还发现,完成重编程后的H3K18cr与早期胚胎第一谱系分化密切相关。在囊胚阶段,H3K18cr在内细胞团(ICM)和滋养外胚层(TE)中呈现不同的富集特征,并与相关谱系决定基因及开放染色质区域相对应,提示其可能在胚胎早期命运决定中发挥预备性调控作用。
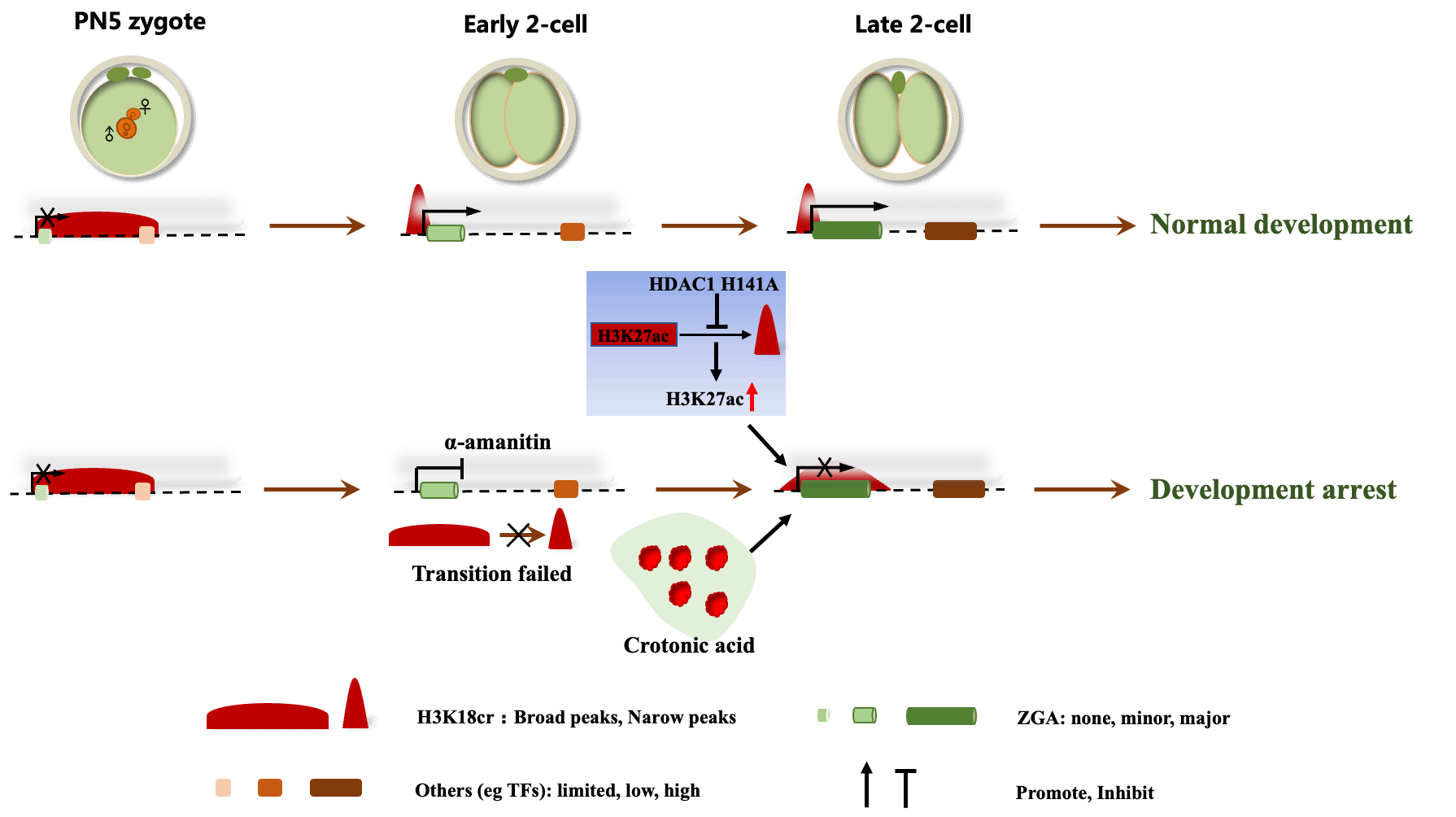
总体而言,该研究揭示了组蛋白巴豆酰化在哺乳动物早期胚胎发育中的动态规律及潜在调控机制,为理解早期胚胎表观遗传重编程提供了新的理论依据,也为生殖发育相关异常的研究提供了新的切入点。广医-广州生物院联合生科院袁慎立和山东大学闫业联为共同第一作者。山东大学吴克良、黄涛和广妇儿刘超、王孝波为共同通讯作者。广医-广州生物院联合生科院为本文第一署名单位。该研究受到了国家重点研发、国家自然科学基金等项目资助。
文章链接:https://pubmed.ncbi.nlm.nih.gov/41933909/
